mozok.click
Вспомните:
• какие растворы называют коллоидными (§ 3);
• какие вещества называют полимерами (§ 28).
Крахмал
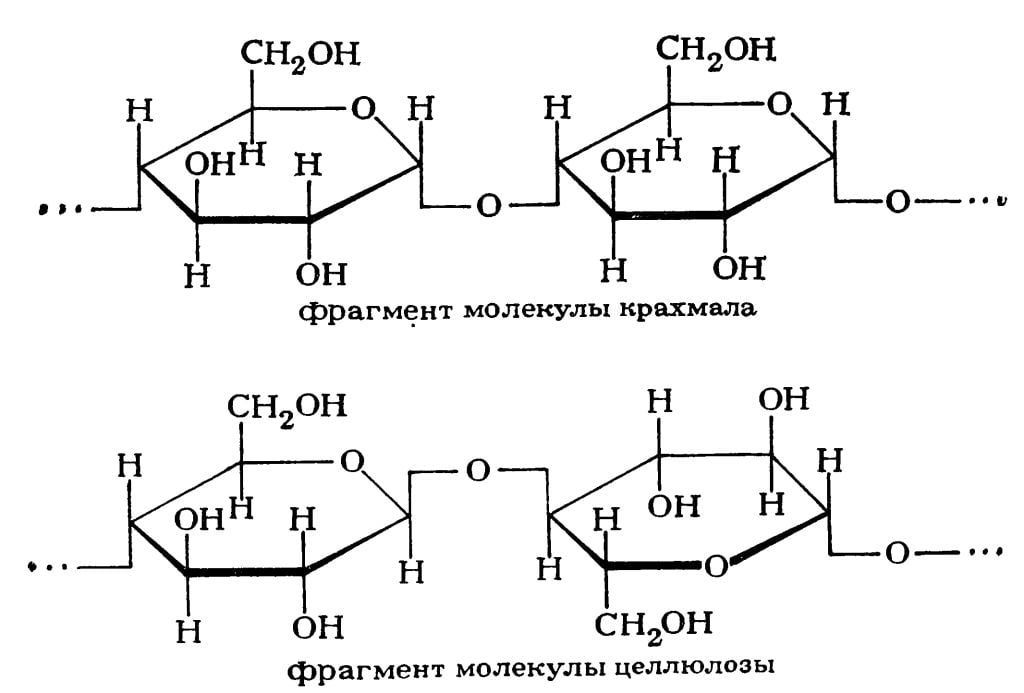
Важнейшими природными полисахаридами являются крахмал и целлюлоза. Оба вещества — полимеры с одинаковой химической формулой: [C6H10O5]n. Отличаются они только строением молекул.
Крахмал — аморфный порошок с характерным хрустом, плотность — 1,5 г/см3, при обычных условиях в воде не растворяется.
При попадании в горячую воду крупинки крахмала поглощают воду и сильно набухают, их оболочки разрушаются и образуется коллоидный раствор. Его называют клейстером и иногда используют в качестве клея.
Температуры плавления и кипения у крахмала нет, поскольку при нагревании он разлагается.
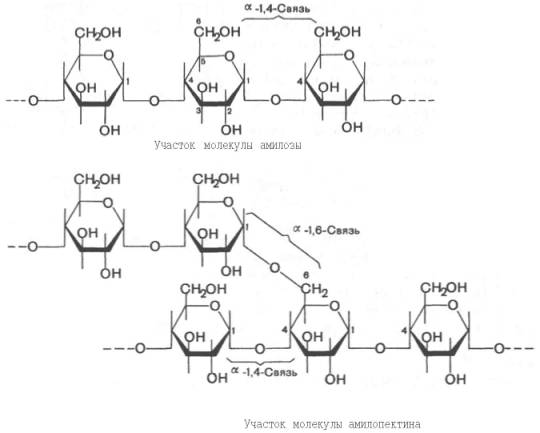
Крахмал состоит из молекул двух типов. Из-за этого иногда говорят, что он состоит из двух веществ: амилозы и амилопектина. У амилозы (ее содержание около 20 %) линейные молекулы (рис. 37.1, а), она лучше растворяется в воде.
Одна молекула амилозы содержит около тысячи остатков молекул глюкозы. Молекулы амилопектина разветвлены и содержат около десятка тысяч остатков молекул глюкозы (рис. 37.1, б). Амилопектин в воде не растворяется, а только набухает.
При длительном нагревании в кислой среде или под действием ферментов крахмал гидролизуется и связи между остатками молекул глюкозы разрываются. Продуктом полного гидролиза крахмала является глюкоза:
Эту реакцию используют в промышленности для изготовления патоки и для получения пищевого этилового спирта.
Наличие крахмала определяют при помощи раствора йода: йод образует с крахмалом соединение синего цвета (рис. 37.2). Используя эту качественную реакцию, можно обнаружить крахмал во многих пищевых продуктах: картофеле, хлебе, кукурузе и др.:
Крахмал образуется в растениях из глюкозы и накапливается в корнях, клубнях и семенах:
Крахмал является основным углеводом нашей пищи. Много крахмала содержится в пшенице и других зерновых культурах, а также муке, которую из них делают. Непосредственно организмом он не усваивается.
Под действием ферментов происходит гидролиз крахмала, который начинается уже при пережевывании пищи во рту, продолжается в желудке и заканчивается в кишечнике. Глюкоза, образующаяся в результате гидролиза, впитывается в кровь и поступает в печень, а оттуда — во все ткани организма.
Избыток глюкозы откладывается в печени в виде полисахарида гликогена, который снова гидролизуется до глюкозы по мере ее расходования в клетках организма.
Большие объемы крахмала идут на производство этилового спирта. Для этого крахмал сначала подвергают гидролизу под действием ферментов солода, а продукт гидролиза после брожения под действием дрожжей превращается в спирт.
Целлюлоза
Целлюлоза (клетчатка) — белое волокнистое вещество, нерастворимое в воде и других растворителях (в отличие от крахмала). Плотность целлюлозы в зависимости от сырья колеблется в пределах от 1,27 до 1,61 г/см3.
Химическая формула целлюлозы такая же, как и у крахмала — [CgH10O5]n.
Но в отличие от крахмала, молекулы целлюлозы не бывают разветвленными и содержат десятки тысяч остатков молекул глюкозы (молекулярная масса целлюлозы достигает нескольких миллионов).
Отдельные макромолекулы целлюлозы располагаются упорядоченно и плотно друг к другу, образуя прочные волокна, что не характерно для крахмала (рис. 37.3).
Целлюлоза взаимодействует с водой, подвергаясь гидролизу при значительно более жестких условиях по сравнению с крахмалом — при длительном кипячении с кислотой. Разумеется, продуктом гидролиза также является глюкоза.
Целлюлозу, а точнее древесину, ее содержащую, используют как топливо. Как и большинство органических веществ, целлюлоза сгорает до углекислого газа и воды:
Рис. 37.3. Молекулы крахмала имеют преимущественно разветвленное строение (а), а молекулы целлюлозы — линейное строение (б)
Целлюлоза — основное вещество растительных клеток: древесина состоит из нее на 50 %, а хлопок и лен — это почти чистая целлюлоза (рис. 37.4). Организм человека и животных (кроме жвачных животных, лошадей и кроликов) не способен переваривать целлюлозу.
Хотя у крахмала и целлюлозы одинаковый химический состав, благодаря разному строению молекул они выполняют различные функции в организме: крахмал — питательное вещество, а целлюлоза — прочный строительный материал.
Основная отрасль, где используют целлюлозу,— бумажная. Бумага, на которой напечатан этот текст, состоит главным образом из целлюлозы, выделяемой из древесины. Целлюлозу используют также
Рис. 37.5. Использование целлюлозы
в производстве искусственных волокон и взрывчатых веществ. Из почти чистой целлюлозы изготавливают очень прочную пленку — целлофан. Путем обработки целлюлозы уксусной кислотой получают ацетилцеллюлозу, из которой изготавливают ацетатное волокно (искусственный шелк), кино- и фотопленку и другие ценные материалы.
Немецкое Kraftmehl («крахмал») произошло от немецких слов Kraft — «сила» и Mehl — «мука», т. е. крахмал — сила муки. Крахмал из картофеля впервые был получен в 1781 году, а до этого его получали из пшеницы.
ЛАБОРАТОРНЫЕ ОПЫТЫ № 13, 14
Оборудование: штатив с пробирками, шпатель, пробиркодержатель, горелка.
Реактивы: вода, крахмал, раствор йода (спиртовой или раствор Люголя).
Правила безопасности:
• для проведения опытов используйте небольшие количества реактивов;
• во время нагревания не прикасайтесь руками к горячим предметам;
• остерегайтесь попадания реактивов на кожу, в глаза, на одежду.
Отношение крахмала к воде
В две пробирки налейте по 2-3 мл воды. Одну из них нагрейте почти до кипения воды. В обе пробирки насыпьте небольшое количество (на кончике шпателя) крахмала и осторожно перемешайте встряхиванием. Сделайте вывод о растворимости крахмала в холодной и горячей воде.
Как называют раствор крахмала в воде? К какому типу дисперсных систем он относится?
Взаимодействие крахмала с йодом
К раствору крахмала, полученному в предыдущем опыте, добавьте одну каплю разбавленного раствора йода (светло-соломенного цвета). Что наблюдаете? Сделайте выводы о признаках качественной реакции на крахмал.
ДОМАШНИЙ ЭКСПЕРИМЕНТ № 3
Определение крахмала в пищевых продуктах
Вам понадобятся: пипетка, стакан, йодная настойка, салициловый спирт (борный, муравьиный) — их можно купить в аптеке или взять в домашней аптечке; любые пищевые продукты с содержанием крахмала: картофельный крахмал, мука, хлеб, пирожные, чипсы, томатный сок, макароны, отвар риса или другой крупы, вареная колбаса (или сосиски), сметана и др.
Правила безопасности:
• для опытов используйте небольшие количества веществ;
• остерегайтесь попадания веществ на кожу, одежду, в глаза; при попадании вещество следует смыть большим количеством воды.
1. Подготовьте раствор йода. Обычно аптечная йодная настойка содержит 5 % йода. Для выявления крахмала такой раствор использовать неудобно: он очень темный, и появление синей окраски при наличии крахмала можно не заметить. Раствор йода необходимо разбавить.
В воде йод не растворяется, поэтому для его растворения нужно использовать этанол (в виде фармацевтических препаратов на его основе). В стакан или флакон влейте примерно две столовые ложки салицилового спирта.
К этому спирту пипеткой добавьте одну (или больше) каплю йодной настойки, чтобы получить раствор светло-соломенного цвета. Этим раствором теперь можно пользоваться для определения крахмала.
2. Исследуйте имеющиеся у вас продукты питания на содержание крахмала. Для этого на небольшие кусочки пипеткой добавьте по несколько капель раствора йода. По изменению окраски сделайте вывод о наличии крахмала в исследуемых продуктах. Результаты опытов оформите в виде таблицы:
Ключевая идея
Полисахариды — это природные полимеры, мономерами которых являются остатки молекул моносахаридов. Самые распространенные из них — крахмал и целлюлоза — полимеры, образованные глюкозой.
Контрольные вопросы
455. Приведите химическую формулу крахмала и целлюлозы. Почему эти углеводы называют полимерами?
456. Чем отличается строение молекул крахмала и целлюлозы?
457. Охарактеризуйте физические свойства крахмала и целлюлозы.
458. Каким образом можно определить наличие крахмала в растворе или других смесях?
459. Опишите применение крахмала и целлюлозы. На каких их свойствах оно основано?
Задания для усвоения материала
460. Опишите, какие процессы происходят при таких превращениях: целлюлоза ^ углекислый газ ^ глюкоза ^ крахмал.
461. Сколько структурных звеньев C6H10O5 содержится в молекуле целлюлозы, если ее относительная молекулярная масса равна 2,1 млн?
462. Вычислите объем целлюлозы количеством вещества 1 моль, если одна молекула целлюлозы содержит в среднем 10 000 остатков молекул глюкозы, а ее плотность — 1,52 г/см3.
463. Для приготовления киселя на 1 л жидкости обычно добавляют 2 столовые ложки крахмала. Вычислите массовую долю крахмала в таком киселе, если в одной столовой ложке содержится около 30 г картофельного крахмала.
464. Вычислите объем углекислого газа, который выделится при полном сгорании ваты массой 1 кг, если считать, что она полностью состоит из целлюлозы. Какой объем кислорода для этого понадобится (н. у.)?
465*. Представьте, что вы работаете химиком в текстильной компании и вам необходимо выполнить исследовательский проект, направленный на применение синтетических заменителей хлопка. Какую информацию вы должны собрать и какие вопросы рассмотреть для решения этой проблемы? Составьте план эксперимента для своего исследования.
466*. Как можно удалить пятно от йодной настойки на ткани, используя для этого срез сырого клубня картофеля?
467*. Как вы считаете, из какого картофеля можно получить больше крахмала: из только что выкопанного или из того, который всю зиму находился в овощехранилище?
ПРАКТИЧЕСКАЯ РАБОТА № 5
Определение органических соединений в пищевых продуктах
Оборудование: штатив с пробирками, шпатель.
Реактивы: образцы пищевых продуктов (ориентировочно): виноград, яблоки, свежее молоко, кефир, творог, виноградный,
апельсиновый и томатный соки; растворы йода, купрум(П) сульфата, щелочи, универсальный индикатор (или индикаторная бумага).
Правила безопасности:
• для проведения опытов используйте небольшие количества веществ;
• остерегайтесь попадания веществ на кожу, одежду, в глаза; при попадании вещество следует смыть большим количеством воды.
Опыт 1. Исследуйте на содержание крахмала кефир, творог и томатный сок. Для определения крахмала к исследуемому образцу следует добавить 1-2 капли раствора йода. Какой признак должен свидетельствовать о наличии крахмала? Опишите ваши наблюдения. Должен ли содержаться крахмал в исследованных продуктах?
Опыт 2. Используя универсальный индикатор, определите значение pH в имеющихся образцах продуктов (для исследования винограда из него следует выжать сок, а небольшой кусок яблока следует измельчить).
Какая среда (кислотная, щелочная или нейтральная) в имеющихся образцах? Какая среда должна быть в этих образцах? Если среда кислотная, предположите, какие органические кислоты содержат эти продукты.
Опыт 3. Исследуйте на содержание глюкозы виноград, яблоки, виноградный и апельсиновый соки (для исследования винограда из него следует выжать сок, а кусочек яблока следует измельчить).
Для определения содержания глюкозы сначала необходимо получить свежеосажденный осадок купрум(П) гидроксида взаимодействием купрум(П) сульфата со щелочью (как вы это делали в Лабораторном опыте № 12, с. 209). Затем к осадку добавлять исследуемый сок до исчезновения осадка.
Опишите свои наблюдения. Во всех ли образцах должна содержаться глюкоза? В каком образце вы обнаружили наличие глюкозы?
Результаты опытов оформите в виде таблицы:
Вывод. Сделайте обобщающий вывод. Для этого используйте ответы на вопросы:
1. Какие реакции называют качественными? На каких признаках основано определение наличия тех или иных веществ в растворе?
2. При помощи каких качественных реакций можно обнаружить глицерол, глюкозу, крахмал?
3. Что общего в строении молекул глицерола и глюкозы?
4. Какие выводы о качестве пищевых продуктов можно сделать, основываясь на результатах опытов?
Это материал учебника Химия 9 класс Григорович
Источник: https://mozok.click/866-uglevody-krahmal-i-cellyuloza.html
Химические и физические свойства крахмала, гликогена и целлюлозы. Указать черты сходства и различия в строении и свойствах
Крахмал, гликоген, целлюлоза — природные высокомолеклярные соединения, образованные остатками глюкозы (несахароподобные полисахариды). Общая формула полисахаридов (С6Н10О5)n.
Крахмал — самый распространенный в природе полисахарид, играющий роль резервного продукта многих растений. В состав крахмала входят два полисахарида — амилоза и амилопектин.
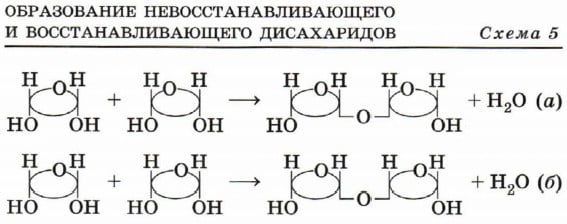
Эти полисахариды построены из остатков α –D- глюкозы, связанных между собой α –(1,4)-глюкозидными связями:
Крахмал — невосстанавливающийся сахар. Гликоген, в отличии от крахмала — восстанавливающий сахар, так как один из циклов содержит сохраненный полуацетальный гидроксил. При химических превращениях эта группа переходит в альдегидную форму и вступает в реакции, характерные для альдегидов. В этом отличие крахмала и гликогена.
Крахмал и гликоген — ценные пищевые продукты.
При гидролизе крахмала и гликогена образуются различные промежуточные продукты:
Гидролизом в присутствии ферментов и последующим брожением из крахиала получают этиловый спирт:
Целлюлоза, или клетчатка — главная составная часть оболочек растительных клеток. Целлюлоза представляет собой полисахарид, который, ак и крахмал с гликогеном, состоит из остатков D-глюкозы. Однако в отличии от них эти остатки связаны между собой β –(1,4)-глюкозидными связями.
Очищенная вата и фильтровальная бумага могут служить образцами почти чистой целлюлозы.
Макромолекулярные цепи целлюлозы имеют линейное строение:
Еще большие отличия между целлюлозой и крахмалом с гликогеном в их свойствах. Целлюлоза — химически инертное вещество. Она не растворима в воде, спирте эфире, ацетоне и других растворителях. Хорошо растворяется в концентрированном растворе хлористого цинка и в реактиве Швейцера.
Целлюлоза не обладает восстановительными свойствами, и труднее . чем крахмал, подвергается гидролизу. Однако при нагревании целлюлозы с минеральными кислотами можно получить промежуточные продукты, вплоть до D-глюкозы:
Химические свойства целлюлозы определяются присутствием в ней трех свободных в цикле гидроксильных групп. Для удобства формулу целлюлозы можно изобразить так: n
Обработка концентрированным раствором щелочи:
С металличесикм натрием образует триалкоголят целлюлозы:
Дает простые и сложные эфиры:
Источник: http://biohimist.ru/kontrolnye-raboty-po-biokhimii/18-biohimija-kontrolnaja-rabota-voprosy-i-otvety/188-himicheskie-i-fizicheskie-svojstva-krahmala.html
Х и м и я
На этой странице мы рассмотрим несахароподобные полисахариды.
Полисахариды — общее название класса сложных высокомолекулярных углеводов, молекулы которых состоят из десятков, сотен или тысяч мономеров — моносахаридов.
Важнейшие представители несахароподобных полисахаридов — крахмал и целлюлоза (клетчатка).
Эти углеводы во многом отличаются от моно- и олигосахаридов. Они не имеют сладкого вкуса, большинство из них не растворимо в воде. По этой причине их называют несахароподобными (в отличие от сахароподобных олигосахаридов, которые также относятся к полисахаридам).
Олигосахариды имеют знаительно меньший размер молекул и свойства, близкие к моносахаридам.
Несахароподобные полисахариды представляют собой высокомолекулярные соединения, которые под каталитическим влиянием кислот или ферментов подвергаются гидролизу с образованием более простых полисахаридов, затем дисахаридов и, в конечном итоге, множества (сотен и тысяч) молекул моносахаридов.
Химическое строение полисахаридов
По химической природе полисахариды стоит рассматривать как полигликозиды (полиацетали). Каждое звено моносахарида связано гликозидными связями с предыдущим и последующим звеньями.
При этом для связи с последующим звеном предоставляется полуацетальная (гликозидная) гидроксильная группа, а с предыдущим — спиртовая гидроксильная группа.
На конце цепи находится остаток восстанавливающегося моносахарида. Но поскольку доля концевого остатка относительно всей макромолекулы весьма невелика, то полисахариды проявляют очень слабые восстановительные свойства.
Гликозидная природа полисахаридов обусловливает их гидролиз в кислой и высокую устойчивость в щелочной средах.
Полисахариды имеют большую молекулярную массу. Им присущ характерный для высокомолекулярных веществ более высокий уровень структурной организации макромолекул.
Наряду с первичной структурой, т.е. определённой последовательностью мономерных остатков, важную роль играет вторичная структура, определяемая пространственным расположением молекулярной цепи.
Классификация полисахаридов
Полисахариды можно классифицировать по разным признакам.
Полисахаридные цепи могут быть:
- разветвлёнными или
- неразветвлёнными (линейными).
Также, различают:
- гомополисахаридами — полисахариды, состоящие из остатков одного моносахарида,
- гетерополисахариды — полисахариды, состоящие из остатков разных моносахаридов.
Наиболее изучены гомополисахариды.
Их можно разделить по их происхождению:
- гомополисахариды растительного происхождения
- гомополисахариды животного происхождения
- гомополисахариды бактериального происхождения
– Крахмалл, – Целюлоза, – Пектиновые вещества и т.д.
– Гликоген, – Хитин и т.д.
– Гекстраны.
Гетерополисахариды, к числу которых относятся многие животные и бактериальные полисахариды, изучены меньше, однако они играют важную биологическую роль.
Гетерополисахариды в организме связаны с белками и образуют сложные надмолекулярные комплексы.
Для полисахаридов используется общее название гликаны.
Гликаны могут быть:
- гексозанами (состоят из гексоз),
- пентозанами, (состоят из пентоз).
В зависимости от природы моносахарида различают:
- глюканы (в основе — моносахарид глюкоза),
- маннаны (в основе — моносахарид манноза),
- галактаны (в основе — моносахарид галактоза) и т.п.
Крахмал
Крахмал (С6Н10О5)n — белый (под микроскопом зернисый) порошок, нерастворимый в холодной воде. В горячей воде крахмал набухает, образуя коллоидный раствор (крахмальный клейстер). С раствором йода даёт синее окрашивание (характерная реакция).
Крахмал образуется в результате фотосинтеза, в листьях растений, и запасается в клубнях, корнях, зёрнах.
Химическое строение крахмала
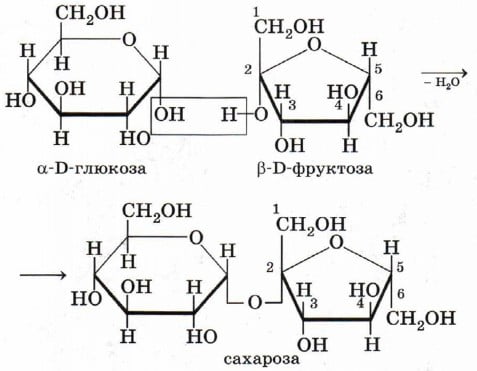
Крахмал представляет собой смесь двух полисахаридов, построенных из глюкозы (D-глюкопиранозы): амилозы (10-20%) и амилопектина (80-90%).
Дисахаридным фрагментом амилозы является мальтоза. В амилозе D-глюкопиранозные остатки связаны альфа(1-4) гликозидными связями.
По данным рентгеноструктурного анализа макромолекула амилозы свёрнута в спираль. На каждый виток спирали приходится 6 моносахаридных звеньев.
Амилопектин в отличие от амилозы имеет разветвлённое строение.
В цепи D-глюкопиранозные остатки связаны альфа(1-4)-гликозидными связями, а в точках разветвления — бета(1-6)-гликозидными связями. Между точками разветвления располагается 20-25 глюкозидных остатков.
Цепь амилозы включает от 200 до 1000 глюкозных остатков, молекулярная масса
160 000. Молекулярная масса амилопектина достигает 1-6 млн.
Гидролитическое расщепление крахмала
В пищеварительном тракте человека и животных крахмал подвергается гидролизу и превращается в глюкозу, которая усваивается организмом.
В технике превращение крахмала в глюкозу (процесс осахаривания) осуществляется путём кипячения его в течение нескольких часов с разбавленной серной кислотой. Впоследствии серную кислоту удаляют.
Получается густая сладкая масса, так называемая крахмальная патока, содержащая, кроме глюкозы, значительное количество других продуктов гидролиза крахмала.
Патока применяется для приготовления кондитерских изделий и различных технических целей.
Если требуется получить чистую глюкозу, то кипячение крахмала ведут дольше. Этим достигается более высокая степень гидролиза крахмала.
При нагревании сухого крахмала до 200-500 град. С происходит частичное разложение его и получается смесь менее сложных, чем крахмал полисахаридов, называемых декстринами.
Разложением крахмала на декстрины объясняется образование блестящей корки на печёном хлебе. Крахмал муки, превращённый в декстрины, легче усваивается вследствие большей растворимости.
Гликоген
В животных организмах этот полисахарид является структурным и функциональным аналогом растительного крахмала.
Откладывается в виде гранул в цитоплазме во многих типах клеток (главным образом печени и мышц).
Химическое строение гликогена
По строению гликоген подобен амилопектину (структурную формулу см. выше). Но молекулы гликогена значительно больше молекул амилопектина и имеют более разветвленную структуру. Обычно между точками разветвления содержится 10-12 глюкозных звеньев, а иногда даже 6.
Сильное разветвление способствует выполнению гликогеном энергетической функции, так как только при наличии большого числа концевых остатков можно обеспечить быстрое отщепление нужного количества молекул глюкозы.
Молекулярная масса у гликогена необычайно велика. Измерения показали, что она равна 100 млн. Такой размер макромолекул содействует выполнению функции резервного углевода. Так, макромолекула гликогена из-за большого размера не проходит через мембрану и остаётся внутри клетки, пока не возникнет потребность в энергии.
Функции гликогена в метаболизме
Гликоген является основной формой хранения глюкозы в животных клетках.
Гликоген образует энергетический резерв, который может быть быстро мобилизован при необходимости восполнить внезапный недостаток глюкозы.
Гликогеновый запас, однако, не столь ёмок в калориях на грамм, как запас триглицеридов (жиров). Он имеет скорее локальное значение. Только гликоген, запасённый в клетках печени (гепатоциты) может быть переработан в глюкозу для питания всего организма.
Гидролиз гликогена в кислой среде протекает очень легко с количественным выходом глюкозы.
Аналогично гликогену в животных организмах, в растениях такую же роль резервного полисахарида выполняет амилопектин, имеющий менее разветвлённое строение.
Меньшая разветвлённость связана с тем, что в растениях значительно медленнее протекают метаболические процессы и не требуется быстрый приток энергии, как это иногда бывает необходимо животному организму (стрессовые ситуации, физическое или умственное напряжение).
Целлюлоза (клетчатка)
Целлюлоза — наиболее распространённый растительный полисахарид. Она обладает большой механической прочностью и выполняет роль опорного материала растений.
Наиболее чистая природная целлюлоза — хлопковое волокно — содержит 85-90% целлюлозы. В древесине хвойных деревьев целлюлозы содержится около 50%.
Химическое строение целлюлозы
Структурной единицей целлюлозы является D-глюкопираноза, звенья которой связаны бета(1-4)-гликозидными связями.
Биозный фрагмент целлюлозы представляет собой целлобиозу. Макромолекулярная цепь не имеет разветвлений, в ней содержится от 2500 до 12 000 глюкозных остатков, что соответствует молекулярной массе от 400 000 до 1-2 млн.
Бета-Конфигурация аномерного атома углерода приводит к тому, что макромолекула целлюлозы имеет строго линейное строение. Этому способствует образование водородных связей внутри цепи, а также между соседними цепями.
Такая упаковка цепей обеспечивает высокую механическую прочность, волокнистость, нерастворимость в воде и химическую инертность, что делает целлюлозу прекрасным материалом для построения клеточных стенок растений.
Целлюлоза не расщепляется обычными ферментами желудочно-кишечного тракта, но она является необходимым для питания баластным веществом.
Использование целлюлозы
Значение целлюлозы очень велико. Достаточно указать, что огромное количество хлопкового волокна идёт для выработки хлопчатобумажных тканей.
Из целлюлозы получают бумагу и картон, а путём химической переработки — целый ряд разнообразных продуктов: искусственное волокно, пластические массы, лаки, этиловый спирт.
Большое практическое значение имеют эфирные производные целлюлозы: ацетаты (искусственный шёлк), ксантогенты (вискозное волокно, целлофан), нитраты (взрывчатые вещества, коллоксилин) и др.
Источник: http://xn—-7sbb4aandjwsmn3a8g6b.xn--p1ai/views/alchemy/theory/chemistry/biochemistry/polysaccharides.php
Крахмал и целлюлоза

ЧАСТЬ И
ОБЩАЯ ХИМИЯ
УГЛЕВОДЫ
Крахмал — это аморфный порошок с характерным хрустом (картофельного крахмала), нерастворимый в воде в обычных условиях. При попадании в горячую воду зерна крахмала сильно набухают, их оболочки разрываются, образуется коллоидный раствор.
Целлюлоза представляет собой волокнистое вещество белого цвета, не растворимый в воде. В отличие от крахмала, целлюлоза совсем не взаимодействует с водой даже йри кипячении. Чистая целлюлоза в нашей жизни встречается в виде ваты.
и целлюлозы
Самая простая формула крахмала (целлюлозы и) — (С6Н10О5)n. В этой формуле значение n — от нескольких сотен до нескольких тысяч. Итак, крахмал — это природный полимер, состоящий из многократно повторяющихся структурных звеньев С6Н10О5. Он состоит из молекул двух типов.
По этой причине крахмал даже считают смесью двух веществ — амилозы и амилопектина. Амилоза (ее в крахмале 20%) имеет линейные молекулы и более растворимая. Молекулы амилопектина (80%) разветвленные, и он менее растворим в воде.
Эти молекулы отличаются и по относительной молекулярной массой: для линейных молекул (амилозы) она достигает порядка сотен тысяч, для разветвленных молекул (амилопектина) — нескольких миллионов.
Самая простая и молекулярная формулы целлюлозы аналогичны формул крахмала. Очевидно, что при одинаковом составе эти вещества существенно отличаются по свойствам. По сравнению с крахмалом у целлюлозы более высокая относительная молекулярная масса.
Причина прочности и нерастворимости целлюлозы заключается в том, что она имеет пространственную трехмерную структуру. Однако целлюлоза не имеет не только трехмерной, но и разветвленной структуры.
Но в этом и заключается причина прочности молекул целлюлозы, потому что они имеют линейную структуру, и отдельные макромолекулы расположены упорядочено плотно друг к другу. Вследствие этого значительно возрастает сила межмолекулярного взаимодействия между отдельными макромолекулами.
Между упорядоченно расположенными макромолекулами целлюлозы устанавливаются многочисленные водородные связи: атомы Кислорода гидроксильных групп одной молекулы электростатически взаимодействуют с атомами Водорода гидроксильных групп другой молекулы.
По этой же причине целлюлоза образует прочные волокна, что не характерно для крахмала. Тем временем в крахмале большинство молекул имеет разветвленную структуру, поэтому возможностей для. установление водородных связей меньше.
Молекулы крахмала состоят из остатков α-глюкозы, а целлюлозы — из остатков молекул β-глюкозы, В этом также заключается причина различий химических свойств крахмала и целлюлозы:
Крахмал
Целлюлоза
Химические свойства крахмала и целлюлозы
1. Комплексообразование крахмала с йодом.
Свойство крахмала образовывать синее окрашивание с йодом используют как качественную реакцию для обнаружения крахмала. С йодом реагирует в основном амилоза, образуя окрашенное соединение. Молекула амилозы в виде спирали окружает молекулы йода, при этом вокруг каждой молекулы йода оказывается шесть глюкозных остатков. Нагревание разрушает такой комплекс, и окраска исчезает.
2. Гидролиз.
Для сахарозы характерна реакция гидролиза. Такая же свойство присуще и крахмала. При длительном кипячении крахмала в присутствии кислоты (чаще всего сульфатной) молекулы подвергаются гидролизу.
Причем конечным продуктом гидролиза есть только α-глюкоза. Однако процесс гидролиза происходит ступенчато с образованием промежуточных продуктов гидролиза.
Ступенчатый процесс гидролиза может быть выражен следующей схеме:
Аналогичную свойство имеет и целлюлоза. Однако гидролиз целлюлозы проходит в более жестких условиях, и конечным продуктом гидролиза является β-глюкоза.
Промежуточные продукты гидролиза целлюлозы не представляют особого интереса, поэтому их можно не указывать и уравнения реакции составлять в суммарном виде:
3. Термическое разложение.
При нагревании древесины до высокой температуры без доступа воздуха выделяется достаточно большое количество продуктов. Кроме углерода и воды, образуются жидкие продукты, в том числе и метиловый спирт (который именно потому и называют древесным спиртом), ацетон, уксусная кислота.
4. Естерифікацїя.
Поскольку остатки глюкозы, входящие в состав целлюлозы, сохраняют гидроксильные группы, то она способна вступать в реакцию эстерификации с кислотами.
В каждом звене целлюлозы содержатся три гидроксильные группы. Все они могут вступать в реакции образования естеріз. В обычной формуле целлюлозы эти гидроксильные группы выделяют так:
Больше всего значение имеют эфиры целлюлозы с нітратною кислотой (нитроцеллюлоза) и уксусной кислотой (ацетилцелюлоза).
Крахмал — это основной углевод нашей пищи; непосредственно он, подобно жиров, организмом не усваивается. Гидролиз крахмала под действием ферментов начинается в рту при пережевывании пищи, продолжается в желудке и кишечнике.
Образована в результате гидролиза глюкоза всасывается в кровь и поступает в печень, а оттуда — во все ткани организма.
Избыток глюкозы откладывается в печени в виде высокомолекулярного углевода гликогена, который снова гидролизуется до глюкозы по мере расходования ее в клетках организма.
Для добывания глюкозы крахмал нагревают с разбавленной серной кислотой в течение нескольких часов. Когда процесс гидролиза закончится, кислоту нейтрализуют мелом, образующийся осадок кальций сульфата отфильтровывают и раствор упаривают. При охлаждении из раствора кристаллизуется глюкоза.
Если процесс гидролиза не доводить до конца, то в результате образуется густая сладкая масса — смесь декстринов и глюкозы — патока.
Декстрины, добытые из крахмала, используют как клей.
Крахмал применяют для накрохмалювання белья под действием нагревания горячим утюгом он превращается в декстрины, которые склеивают волокна ткани и образуют плотную пленку, предохраняющую ткань от быстрого загрязнения. Кроме того, это облегчает следующее стирки, поскольку частички грязи, связанные с декстринами, значительно легче смываются водой.
Крахмал используют для производства этилового спирта. Во время этого процесса его сначала гидролизуют под действием фермента, который содержится в солоде, а потом продукт гидролиза сбраживают в присутствии дрожжей в спирт.
Этиловый спирт, который используют для промышленных нужд (синтез каучука), добывают синтетическим путем из этилена и гидролизом целлюлозы.
Благодаря своей механической прочности целлюлоза в составе древесины используется в строительстве, из нее изготовляют всевозможные столярные изделия. В виде волокнистых материалов (хлопка, льна, конопли), ее используют для изготовления нитей, тканей, канатов. Выделенная из древесины (освобожденная от сопутствующих веществ), целлюлоза идет на изготовление бумаги.
Эстеры целлюлозы используют для изготовления нитролаков, кинопленки, медицинского коллодия, искусственного волокна и взрывчатых веществ.
Источник: http://schooled.ru/chemistry/zno/183.html
Целлюлоза (стр. 1 из 2)
Строение.
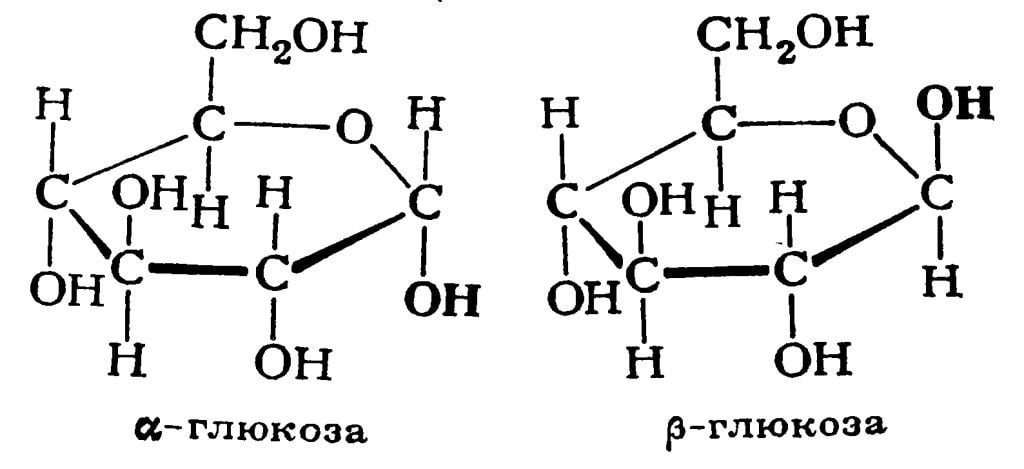
Молекулярная формула целлюлозы (-C6 H10 O5 -)n , как и у крахмала. Целлюлоза тоже является природным полимером. Ее макромалекула состоит из многих остатков молекул глюкозы. Может воэникнуть вопрос: почему крахмал и целлюлоза — вещества с одинаковой молекулярной формулой — обладают различными свойствами?
При рассмотрении синтетических полимеров мы уже выяснили, что их свойства зависят от числа элементарных звеньев и их структуры. Это же положение относится и к природным полимерам. Оказывается, степень полимеризации у целлюлозы намного больше, чем у крахмала.
Кроме того, сравнивая структуры этих природных полимеров, установили, что макромолекулы целлюлозы, в отличие от крахмала, состоят из остатков молекулы b-глюкозы и имеют только линейное строение.
Макромолекулы целлюлозы располагаются в одном направлении и образуют волокна (лен, хлопок, конопля).
В каждом остатке молекулы глюкозы содержатся три гидроксильные группы.
Физические свойства .
Целлюлоза — волокнистое вещество. Она не плавится и не переходит в парообразное состояние: при нагревании примерно до 350о С целлюлоза разлагается — обугливается. Целлюлоза нерастворима ни в воде, ни в большинстве других неорганических и органических растворителях.
Неспособность целлюлозы растворяться в воде — неожиданное свойство для вещества, содержащего по три гидроксильные группы на каждые шесть атомов углерода. Хорошо известно, что полигидроксильные соединения легко растворяются в воде.
Нерастворимость целлюлозы объясняется тем, что ее волокна представляют собой как бы «пучки» расположенных параллельно нитевидных молекул, связанных множеством водородных связей, которые образуются в результате взаимодействия гидроксильных групп.
Внутрь подобного «пучка» растворитель проникнуть не может, а следовательно, не происходит и отрыва молекул друг от друга.
Растворителем целлюлозы является реактив Швейцера — раствор гидроксида меди (II) с аммиаком, с которым она одновременно и взаимодействует. Концентрированные кислоты (серная, фосфорная) и концентрированный раствор хлорида цинка также растворяют целлюлозу, но при этом происходит ее частичный распад (гидролиз), сопровождающийся уменьшением молекулярной массы.
Химические свойства .
Химические свойства целлюлозы определяются прежде всего присутствием гидроксильных групп. Действуя металлическим натрием, можно получить алкоголят целлюлозы [C6 H7 O2 (ONa)3 ]n.
Под действием концентрированных водных растворов щелочей происходит так называемая мерсиризация — частичное образование алкоголятов целлюлозы, приводящая к набуханию волокна и повышению его восприимчивости к красителям. В результате окисления в макромолекуле целлюлозы появляется некоторое число карбонильных и карбоксильных групп.
Под влиянием сильных окислителей происходит распад макромолекулы. Гидроксильные группы целлюлозы способны алкилироваться и ацилироваться, давая простые и сложные эфиры.
Одно из наиболее характерных свойств целлюлозы — способность в присутствии кислот подвергаться гидролизу с образованием глюкозы. Аналогично крахмалу гидролиз целлюлозы протекает ступенчато. Суммарно этот процесс можно изобразить так:
(C6 H10 O5 )n + nH2 O H2SO4_ nC6 H12 O6
Так как в молекулах целлюлозы имеются гидроксильные группы, то для нее характерны реакции этерификации. Из них практическое значение имеют реакции целлюлозы с азотной кислотой и ангидридом уксусной кислоты.
При взаимодействии целлюлозы с азотной кислотой в присутствии концентрированной серной кислоты, в зависимости от условий образуются динитроцеллюлоза и тринитроцеллюлоза, являющиеся сложными эфирами:
При взаимодействии целлюлозы с уксусным ангидридом (в присутствии уксусной и серной кислот) получается триацетилцеллюлоза или диацетилцеллюлоза:
Целлюлоза горит. При этом образуются оксид углерода (IV) и вода.
При нагревании древесины без доступа воздуха происходит разложение целлюлозы и других веществ. При этом получаются древесный уголь, метан, метиловый спирт, уксусная кислота, ацетон и другие продукты.
Получение.
Образцом почти чистой целлюлозой является вата, полученная из очищенного хлопка. Основную массу целлюлозы выделяют из древесины, в которой она содержится вместе с другими веществами. Наиболее распространенным методом получения целлюлозы в нашей стране является так называемый сульфитный.
По этому методу измельченную древесину в присутствии раствора гидросульфита кальция Ca(HSO3 )2 или гидросульфита натрия NaHSO3 нагревают в автоклавах при давлении 0,5–0,6 МПа и температуре 150о С. При этом все другие вещества разрушаются, а целлюлоза выделяется в сравнительно чистом виде.
Ее промывают водой, сушат и направляют на дальнейшую переработку, большей частью на производство бумаги.
Применение.
Целлюлоза используется человеком с очень древних времен. Сначала применяли древесину как горючий и строительный материал; затем хлопковые, льняные и другие волокна стали использовать как текстильное сырье. Первые промышленные способы химической переработки древесины возникли в связи с развитием бумажной промышленности.
Бумага — это тонкий слой волокон клетчатки, спрессованных и проклеенных для создания механической прочности, гладкой поверхности, для предотвращения растекания чернил.
Первоначально для изготовления бумаги употребляли растительное сырье, из которого чисто механически можно было получить необходимые волокна, стебли риса (так называемая рисовая бумага), хлопка, использовали также изношенные ткани.
Однако по мере развития книгопечатания перечисленных источников сырья стало не хватать для удовлетворения растущей потребности бумаги. Особенно много бумаги расходуется для печатания газет, причем вопрос о качестве (белизне, прочности, долговечности) для газетной бумаги значения не имеет.
Зная, что древесина примерно на 50% состоит из клетчатки, к бумажной массе стали добавлять размолотую древесину. Такая бумага непрочна и быстро желтеет (особенно на свету).
Для улучшения качества древесных добавок к бумажной массе были предложены различные способы химической обработки древесины, позволяющие получить из нее более или менее чистую целлюлозу, освобожденную от сопутствующих веществ — лигнина, смол и других. Для выделения целлюлозы было предложено несколько способов, из которых мы рассмотрим сульфитный.
По сульфитному способу измельченную древесину ”варят “ под давлением с гидросульфитом кальция. При этом сопутствующие вещества растворяются, и освобожденную от примесей целлюлозу отделяют фильтрованием.
Образующиеся сульфитные щелока являются в бумажном производстве отходами.
Однако вследствие того, что они содержат наряду с другими веществами способные к брожению моносахариды, их используют как сырье для получения этилового спирта (так называемый гидролизный спирт).
Целлюлоза применяется не только как сырье в бумажном производстве, но идет еще и на дальнейшую химическую переработку. Наибольшее значение имеют простые и сложные эфиры целлюлозы.
Так, при действии на целлюлозу смесью азотных и серных кислот получают нитраты целлюлозы. Все они горючи и взрывчаты.
Максимальное число остатков азотной кислоты, которые можно ввести в целлюлозу, равно трем на каждое звено глюкозы:
[C6 H7 O2 (OH)3 ]n HNO3_ [C6 H7 O2 (ONO2 )3 ]n
Продукт полной этерификации — тринитрат целлюлозы (тринитроцеллюлоза) — должен содержать в соответствии с формулой 14,1% азота.
На практике получают продукт с несколько меньшим содержанием азота (12,5/13,5%), известный в технике под названием пирокселин.
При обработке эфиром пироксилин желатинизируется; после испарения растворителя остаётся компактная масса. Мелконарезанные кусочки этой массы — бездымный порох.
Продукты нитрования, содержащие около 10% азота, отвечает по составу динитрату целлюлозы: в технике такой продукт известен под названием коллоксилин. При действии на него смеси спирта и эфира образуется вязкий раствор, так называемый коллодий, применяемый в медицине.
Если к такому раствору добавить камфору (0.4 ч. камфоры на 1 ч. коллоксилина) и испарить растворитель, то останется прозрачная гибкая плёнка — целлулоид. Исторически — это первый известный тип пластмассы.
Ещё с прошлого века целлулоид получил широкое применение как удобный термопластичный материал для производства многих изделий (игрушки, галантерея и т. д.). В особенности важно использование целлулоида в производстве киноплёнки и нитролаков.
Серьёзным недостатком этого материала является его горючесть, поэтому в настоящее время целлулоид всё чаще заменяют другими материалами, в частности ацетатами целлюлозы.
Источник: http://MirZnanii.com/a/324502/tsellyuloza
Урок №64. Глюкоза, сахароза — важнейшие представители углеводов. Крахмал и целлюлоза — природные полимеры. — ХиМуЛя.com
УГЛЕВОДЫ
Углеводы входят в состав клеток и тканей всех растительных и животных организмов и по массе составляют основную часть органического вещества на Земле. На долю углеводов приходится около 80% сухого вещества растений и около 20% животных. Растения синтезируют углеводы из неорганических соединений — углекислого газа и воды (СО2 и Н2О) в процессе фотосинтеза:
6СО2 + 6Н2О свет, хлорофилл→ C6H12O6 + 6O2
Углеводы имеют общую формулу Cn(H2O)m, откуда и возникло название этих природных соединений. Углеводы делятся на: моносахариды (важнейшие представители — глюкоза и фруктоза); дисахариды (сахароза); полисахариды (важнейшие представители — крахмал и целлюлоза).
Пищевые продукты, насыщенные углеводами
Глюкоза C6H12O6– наиболее важный из всех моносахаридов, так как она является структурной единицей большинства пищевых ди- и полисахаридов.
В процессе обмена веществ они расщепляются на отдельные молекулы моносахаридов, которые в ходе многостадийных химических реакций превращаются в другие вещества и в конечном итоге окисляются до углекислого газа и воды — используются как «топливо» для клеток.
Глюкоза — необходимый компонент обмена углеводов. При снижении ее уровня в крови или высокой концентрации и невозможности использования, как это происходит при диабете, наступает сонливость, может наступить потеря сознания (гипогликемическая кома).
Она содержится в плодах и ягодах и необходима для снабжения энергией и образования в печени гликогена (запасной углевод человека и животных).
Особенно её много в виноградном соке, поэтому глюкозу иногда называют виноградным сахаром. Мёд в основном состоит из смеси глюкозы с фруктозой.
Глюкоза является ценным питательным продуктом. В организме она подвергается сложным биохимическим превращениям, в результате которых образуется диоксид углерода и вода, при этом выделяется энергия согласно итоговому уравнению:
C6H12O6 + 6O2 → 6H2O + 6CO2 + 2800 кДж
Так как глюкоза легко усваивается организмом, её используют в медицине в качестве укрепляющего лечебного средства при явлениях сердечной слабости, шоке, она входит в состав кровозаменяющих и противошоковых жидкостей. Широко применяют глюкозу в кондитерском деле (изготовление мармелада, карамели, пряников и т.
д.), в текстильной промышленности в качестве восстановителя, в качестве исходного продукта при производстве аскорбиновой кислоты, для синтеза ряда производных сахаров и т.д. Большое значение имеют процессы брожения глюкозы.
Так, например, при квашении капусты, огурцов, молока происходит молочнокислое брожение глюкозы, так же как и при силосовании кормов. Если подвергаемая силосованию масса недостаточно уплотнена, то под влиянием проникшего воздуха происходит маслянокислое брожение и корм становится непригоден к применению.
На практике используется также спиртовое брожение глюкозы, например при производстве пива.
Применение глюкозы
Фруктоза C6H12O6является одним из самых распространенных углеводов фруктов, содержится в мёде. В отличие от глюкозы она может без участия инсулина проникать из крови в клетки тканей. По этой причине фруктоза рекомендуется в качестве наиболее безопасного источника углеводов для больных диабетом.
Сахароза С12Н22О11, образован молекулами глюкозы и фруктозы. Содержание сахарозы в сахаре 99,5%. Сахар часто называют «носителем пустых калорий», так как сахар — это чистый углевод и не содержит других питательных веществ, таких, как, например, витамины, минеральные соли. Сахароза содержится в сахарном тростнике и сахарной свекле, а также в сладостях.
Сбор сахарного тростника. Фреска во дворце Кортеса в Куэрнаваке.
Крахмал и целлюлоза
Крахмал(С6Н10О5)n — природный полимер, он накапливается в виде зерен, главным образом в клетках семян, луковиц, клубней, а также в листьях и стеблях. Крахмал — белый порошок, нерастворимый в холодной воде.
В горячей воде он набухает и образует клейстер.
Крахмал чаще всего получают из картофеля. Для этого картофель измельчают, промывают водой и перекачивают в большие сосуды, где происходит отстаивание.
Полученный крахмал еще раз промывают водой, отстаивают и сушат в струе теплого воздуха.
Крахмал — основная часть важнейших продуктов питания: муки (75 — 80%), картофеля (25%), саго и др. Энергетическая ценность около 16,8 кДж/г. Он является ценным питательным продуктом. Чтобы облегчить его усвоение, содержащие крахмал продукты подвергают действию высокой температуры, то есть картофель варят, хлеб пекут.
В этих условиях происходит частичный гидролиз крахмала и образуются декстрины, растворимые в воде. Декстрины в пищеварительном тракте подвергаются дальнейшему гидролизу до глюкозы, которая усваивается организмом. Избыток глюкозы превращается в гликоген (животный крахмал).
Состав гликогена такой же, как у крахмала, — (C6H10O5)n, но его молекулы более разветвленные. Особенно много гликогена содержится в печени (до 10%). В организме гликоген является резервным веществом, которое превращается в глюкозу по мере ее расходования в клетках.
В промышленности крахмал путем гидролиза превращают в патоку и глюкозу.
Для этого его нагревают с разбавленной серной кислотой, избыток которой затем нейтрализуют мелом.
(С6Н10О5)n + nH2O –H2SO4, t˚C→nC6H12O6
Образовавшийся осадок сульфата кальция отфильтровывают, раствор упаривают и выделяют глюкозу. Если гидролиз крахмала не доводить до конца, то образуется смесь декстринов с глюкозой — патока, которую применяют в кондитерской промышленности. Получаемые с помощью крахмала декстрины используются в качестве клея, для загустения красок при нанесении рисунков на ткань.
Крахмал применяют для накрахмаливания белья. Под горячим утюгом происходит частичный гидролиз крахмала и превращение его в декстрины. Последние образуют на ткани плотную пленку, которая придает блеск ткани и предохраняет ее от загрязнения.
Крахмал и его производные применяются при производстве бумаги, текстильных изделий, в литейном и других производствах, в фармацевтической промышленности.
Изучение физических свойств крахмала
Обнаружение крахмала
Целлюлоза или клетчатка (С6Н10О5)n , один из самых распространённых природных полимеров; главная составная часть клеточных стенок растений, обусловливающая механическую прочность и эластичность растительных тканей. Так, содержание целлюлозы в волосках семян хлопчатника 97—98%, в стеблях лубяных растений (лён, рами, джут) 75—90%, в древесине 40—50%, камыше, злаках, подсолнечнике 30—40%. Обнаружена в организме некоторых низших беспозвоночных.
Целлюлоза используется человеком с очень древних времен. Сначала применяли древесину как горючий и строительный материал; затем хлопковые, льняные и другие волокна стали использовать как текстильное сырье. Первые промышленные способы химической переработки древесины возникли в связи с развитием бумажной промышленности.
Бумага — это тонкий слой волокон клетчатки, спрессованных и проклеенных для создания механической прочности, гладкой поверхности, для предотвращения растекания чернил.
Первоначально для изготовления бумаги употребляли растительное сырье, из которого чисто механически можно было получить необходимые волокна, стебли риса (так называемая рисовая бумага), хлопка, использовали также изношенные ткани.
Однако по мере развития книгопечатания перечисленных источников сырья стало не хватать для удовлетворения растущей потребности бумаги. Особенно много бумаги расходуется для печатания газет, причем вопрос о качестве (белизне, прочности, долговечности) для газетной бумаги значения не имеет.
Зная, что древесина примерно на 50% состоит из клетчатки, к бумажной массе стали добавлять размолотую древесину. Такая бумага непрочна и быстро желтеет (особенно на свету).
Для улучшения качества древесных добавок к бумажной массе были предложены различные способы химической обработки древесины, позволяющие получить из нее более или менее чистую целлюлозу, освобожденную от сопутствующих веществ — лигнина, смол и других.
Для выделения целлюлозы было предложено несколько способов, из которых мы рассмотрим сульфитный. По сульфитному способу измельченную древесину ”варят “ под давлением с гидросульфитом кальция. При этом сопутствующие вещества растворяются, и освобожденную от примесей целлюлозу отделяют фильтрованием. Отходы содержат способные к брожению моносахариды, их используют как сырье для получения этилового спирта (так называемый гидролизный спирт). Целлюлоза используется для получения вискозного, ацетатного, медно-аммиачного волокон.
Задания для закрепления
№1.
Источник: https://sites.google.com/site/himulacom/zvonok-na-urok/9-klass—vtoroj-god-obucenia/urok-no64-glukoza-saharoza-vaznejsie-predstaviteli-uglevodov-krahmal-i-celluloza-prirodnye-polimery
американский сигареты парламент в России.




